(一)材料与方法
小白鼠骨髓瘤细胞株SP2/0(医科院基础所细胞生物学研究室),进行传带培养,在对数生长期,将细胞打起,吸取适量细胞悬液,均匀分配至一6孔板(CORNING)中,此培养板预先用自制的大白鼠鼠尾胶原包被,每孔加4ml 15%FCS RPMI1640培养液。设定上三孔为实验孔,下三孔为对照孔,培养14h后,每个实验孔加再生物质约1g,对照孔加等量RPMI1640培养液。培养后44h后,进行下列项目的检测。
1、观察实验组和对照组细胞的镜下形态。
2、实验组和对照组细胞用苏木精-伊红染色(HE染色) 预先配制好染色用全套试剂,并将蛋清/甘油粘片剂涂于洁净载玻片上,吹风机吹干;在培养SP2/0细胞的6孔培养板中,将每个孔的细胞打起,每孔各取1ml至Epp管中,这样得到三个实验组样本和三个对照组样本,用于下述“3”中的荧光读数的检测。将三个实验孔中的剩余部分和三个对照孔中的剩余部分合成一个实验样品和一个对照样品,然后将此实验样品和对照样品一分为二,得到两个实验样品和两个对照样品,然后取其中的一对实验样品和对照样品,进行下述“4”中的荧光显微镜检测,取另一对实验样品和对照样品进行下述的HE染色,HE染色过程为:(1)首先将实验样品和对照样品的细胞悬液分别移至Epp管中;(2)水平转头离心,1500转/分钟,离心5分钟,弃上清,留约10ul;(3)混悬细胞,制成细胞悬液;(4)将上述制备好的微量细胞悬液,加至载玻片上,用希耳球吹匀平摊;(5)干燥至无水分为止;(6)染色过程:10%甲醛固定10分钟,水洗;苏木精染色2分钟,水洗30秒;1%盐酸酒精分化20秒,自来水洗20秒;稀氨水30秒,自来水洗20秒;伊红染色1分钟,水洗10秒;85%酒精20秒;90%酒精30秒;95%酒精1分钟;无水乙醇Ⅰ1分钟;无水乙醇Ⅱ2分钟;二甲苯Ⅰ1分钟;二甲苯Ⅱ1分钟;中性树胶盖玻片封固;37℃烤干。结果照相记录保存。
3、检测经过培养的实验组和对照组细胞的荧光值,以判断细胞增殖的程度 具体方法如下:(1)将“3”中所述的三个实验组样本和三个对照组样本水平转头离心,2000转/分钟,离心5分钟,吸弃干净上清;(2)加20μl吖啶橙基液,再加1mlPBS,(3)振荡混匀,室温5分钟;(4)离心,条件同上;(5)弃净上清,每孔加100μlPBS,混匀;(6)将各孔的细胞悬液加至96孔LABSYSTEMS CLINIPLATE标准检测板中,至此有三个实验孔,三个对照孔,另设三个PBS空白对照孔;(7)用荧光/化学发光仪检测荧光,条件为激发光波长485nm,发射光波长527nm,检测值与DNA量成正比,间接反映细胞数量。
4、吖啶橙荧光染色 (1)将“2”中所述的一对实验样品和对照样品水平转头离心,2000转/分钟,离心5分钟,吸弃干净上清;(2)加20μl吖啶橙基液,再加1mlPBS;(3)振荡混匀,室温5分钟;(4)离心,条件同上;(5)弃净上清,每孔加20μlPBS,混匀;(6)实验样品和对照样品加至同一玻片的两端,盖玻片盖好;(7)用荧光显微镜检测,检测条件为EX450-490/BA520,结果照相记录保存。
(二)结果
1、活细胞形态观察。实验组SP2/0细胞在加药后形态很快发生了非常明显的改变,对照组细胞生长正常,形态正常。
2、HE检测。通过HE染色检查细胞形态和结构的完整性。HE染色显示,实验组典型细胞极少,而对照组细胞均正常。
 |
 |
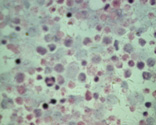
| 3A(×400) |
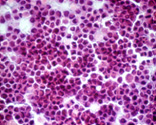
3B(×400) |
图3 培养后第2天实验组和对照组培养孔细胞经HE染色后形态比较,此时实验组已经加药32小时。3A为实验组,3B为对照组。实验组典型细胞极少,形态及着色异常;而对照组细胞形态典型,着色正常,细胞大,细胞核大,细胞浆少,核浆比例增大。 |
3、荧光读数检测,荧光读数反映了细胞内DNA的量,DNA浓度越高,检测值越高,说明细胞数量多,增殖程度高,反之则说明细胞数量少,增殖程度低。本实验显示实验组检测值低于对照组,说明与对照组相比实验组细胞数量少,增殖程度低。表1和图4为荧光读数结果统计表和图解。统计结果显示,实验组和对照组差异显著,说明实验组细胞少,对照组细胞多,结合其它检测结果,说明实验组细胞严重生长不良。
表1 检测结果统计 |
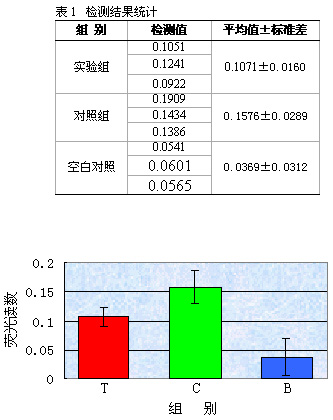 |
图4 为表1的统计结果直方图。T:实验组;C:对照组; B:空白对照组 |
4、荧光染色。荧光染色过程中,荧光染料吖啶橙与DNA、RNA都有亲合力,但结合后却发不同颜色的荧光,在荧光显微镜下,使得细胞核呈亮绿色,而细胞浆呈绿色。实验结果显示,实验组细胞无上述表现,而对照组细胞有上述表现,说明实验组细胞是死细胞或趋于死亡的细胞,而对照组细胞是活细胞。结果见下图。
|
